11月13日,普米斯生物本事公司(以下简称“普米斯”),晓喻与BioNTech终了股权收购条约。
把柄条约条件,BioNTech将以8亿好意思元(约57.81亿元东谈主民币)预支款收购普米斯100%已刊行股本(可把柄老例对收购价钱进行调整),支付式样主要为现款和部分好意思国存托股份(ADS)。此外,BioNTech将在普米斯达到两边商定的里程碑条件时,非常支付最高1.5亿好意思元(约10.84亿元东谈主民币)的里程碑付款。该交游展望于2025年第一季度完成,具体取决于按老例完成交割条件和监管部门的批准。
本次交游完成后,BioNTech将得回普米斯候选药物管线过头双特异性抗体药物斥地平台的一谈职权,进一步扩大其在中国的业务边界;普米斯珠海将算作BioNTech中国研发中心开展关连R&D询查;合适海外程序的普米斯南通出产基地将为BioNTech改日的群众居品出产和供应作念出孝顺;逾300名普米斯研发、出产和复旧职能部门职工加入BioNTech。
与普米斯协作的双抗进展优异
这次并购建立在两边旧年两次协作之上。
2023年7月,BioNTech与普米斯生物终了过政策询查协作、面貌引进聘请以及群众许可条约。把柄该条约条件,BioNTech将得回普米斯用于休养恶性肿瘤的一款临床前询查阶段双特异性抗体和一款临床询查阶段单克隆抗体的群众独家聘请权。此外,普米斯将多个在研临床前纳米抗体面貌专属授权给BioNTech,并把柄其需求提供指定靶向纳米抗体斥地服务。
短短四个月后,两边再次终了协作。BioNTech以5500万好意思元的首付款,及超10亿好意思元的斥地、注册和贸易里程碑付款以及分级销售提成,得回普米斯抗PD-L1/VEGF双特异性抗体(PM8002)在群众(大中华区之外)的斥地、出产和贸易化职权。
PM8002是一款双特异性抗体药物,由东谈主源化的抗PD-L1单域抗体(VHH)交融到一个含有Fc-千里默突变的抗VEGF-A IgG1抗体上组成,现已在国内开展针对TNBC、小细胞肺癌、非小细胞肺癌、宫颈癌等多个瘤种的多项临床询查。
夙昔12月,普米斯便在第46届圣安东尼奥乳腺癌商酌会(SABCS)公布了PM8002与化疗连合休养三阴性乳腺癌(TNBC)的疗效收尾。收尾炫夸,限制2023年6月30日,共有42例患者接纳了休养,并至少进行了一次疗效评估。药物知道的中位合手续时刻为4.6个月(边界:2.0至7.6个月)。最好总体ORR为78.6%(33/42),包括1例十足缓解(CR)和32例部分缓解(PR),其中29例在患者初度评估时即得回缓解。证据的ORR为71.4%,总体疾病划定率(DCR)为95.2%。中位至缓解时刻(TTR)为1.9个月(95%CI:1.8~2.0)。中位筹办病变最好百分比变化为-47.2%(第一四分位数、第三四分位数:-56.9%,-33.5%)。中位缓解合手续时刻(DOR)为7.2个月,中位无进展生计期(PFS)为9.2个月。

本年以来,PM8002临床进展更是喜报频传。3月,PM8002被国度药监局药品审评中心(CDE)纳入冲破性休养品种,针对恰当症为连合打针用白卵白联接型紫杉醇一线休养不能手术的局部晚期/复发飘浮性三阴性乳腺癌。
4月底,PM8002获国度药品监督处罚局(NMPA)批准开展一项注册性III期临床磨练:PM8002打针液或劝慰剂连合打针用白卵白联接型紫杉醇一线休养不能手术的局部晚期/复发飘浮性三阴性乳腺癌(TNBC)的多中心、立时、双盲III期临床询查。后又讲求在Clinicaltrials.gov网站上注册了PM8002(20mg/kg Q2W)连合化疗一线休养局部晚期或飘浮性三阴乳腺癌的III期临床磨练。
几天后,BioNTech便晓喻利用第一次政策协作的群众独家聘请权,得回由普米斯自主研发的临床前双特异性抗体候选药物的群众斥地、出产和贸易化职权。
据2024年BioNTech第三季度财报表现,本年10月,BNT327/PM8002针对乳腺癌的Ⅱ期临床磨练完成了首例患者给药,旨在评估该居品在两个剂量水平下与化疗连合使用,在一线和二线休养局部晚期/飘浮性三阴乳腺癌(TNBC)患者的安全性、疗效和药代能源学。
小细胞肺癌方面,BioNTech晓喻已于9月完成针对小细胞肺癌的Ⅱ期临床磨练的首例患者给药,旨在评估BNT327/PM8002与化疗连合在未经休养的闲居期小细胞肺癌患者中的疗效,以及在接纳一线或二线休养后进展的小细胞肺癌患者中的疗效。另一边,普米斯也在9月开动了一项III期临床,以评估PM8002连合紫杉醇对比化疗二线休养小细胞肺癌的灵验性和安全性。
10条临床询查阶段管线,正入部下手搭建ADC本事平台
在PM8002之外,普米斯还正在鼓动超20个1类生物新药面貌,其中多个新药面貌处于临床询查阶段。公司在珠海、苏州和香港设有新药研发中心,并在上海、北京设立临床询查中心,在南通建造产业化出产基地。普米斯的中枢团队领有逾越20年的高端生物新药研发、居品讲述及上市教师。
从本事平台来看,普米斯在抗体发现、抗体工程纠正、发现生物学、临床前、CMC询查各才气均建有中枢本事平台,复旧抗体新药面貌从抗体发现到临床讲述的全经过。
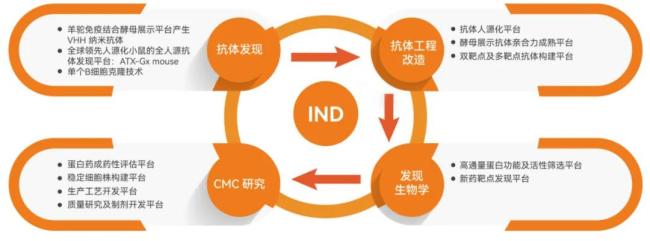
图源:普米斯官网
在候选管线方面,限制当今,普米斯已有10个抗体新药面貌正处于临床询查阶段,并有多项临床磨练处于Ⅱ期。
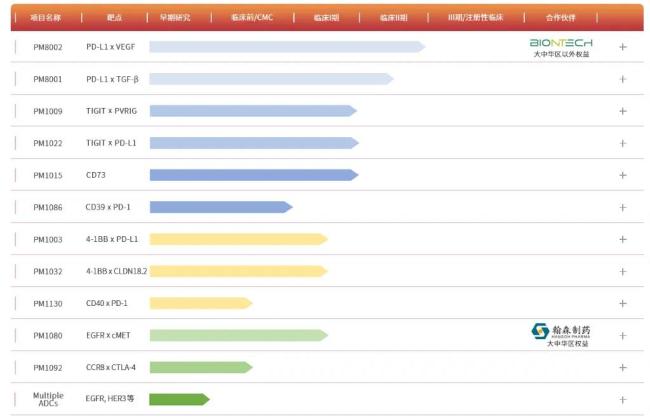
图源:普米斯官网
除与BioNTech终了协作外,普米斯还与多个药企终了政策协作。境外来看,本年齿首,普米斯与好意思国Bitterroot Bio终了政策协作,共同研发可用于颐养免疫系统和调控炎症响应的双功能卵白类新药,从而达到休养多种心血管疾病的成果。
国内方面,普米斯与翰森制药自2022年协作后再一次扩大政策协作关系,许可翰森制药使用普米斯自主研发的抗EGFR/cMet双特异性抗体PM1080/HS-20117用于斥地抗体药物偶联物(ADC)居品,普米斯则将将得回翰森制药支付的首付款和基于ADC居品的斥地、注册及基于销售的贸易化里程碑潜在付款,料想不逾越50亿元东谈主民币,以及基于群众净销售额的分级特准权使用费。
而这也可以调皮视为普米斯向ADC探索的第一步。这次协作中,普米斯连合首创东谈主、董事长兼首席实行官刘晓林曾示意,这次协作将普米斯在双抗新药斥场地面的上风和翰森制药的ADC斥地上风联接起来,有望斥地出临床成果更优的PM1080-ADC新药。
ADC是现时国产新药出海的热点品种之一,刘晓林在此前接纳21世纪经济报谈的采访中示意,当今普米斯如故入部下手搭建ADC平台,并觉得“跟着精确休养期间的到来,ADC将会替代化疗,改日‘IO(肿瘤免疫疗法)+ADC’连合用药具有庞杂的思象空间……下一个阶段的ADC药物斥地又会回到关连抗体的生物学机制上,抗体包括单抗,双抗等的功能可能会起到更重要的作用,而抗体研发是咱们的执意,普米斯有可能在这个规模领略更多的作用。”
对中国Biotech“如获至宝”的BioNTech
在旧年七次牵手中国Biotech之后,对中国Biotech“如获至宝”的BioNTech不仅有“上新”还有“复购”。包括与宜联生物终了多靶点TMALIN®ADC本事平台授权条约,进一步拓展群众政策协作伙伴关系以及与3D打印药物企业三迭纪终了询查协作与平台本事许可条约等。限制当今,BioNTech如故与6家中国Biotech终了协作,多项交游金额超10亿好意思元。
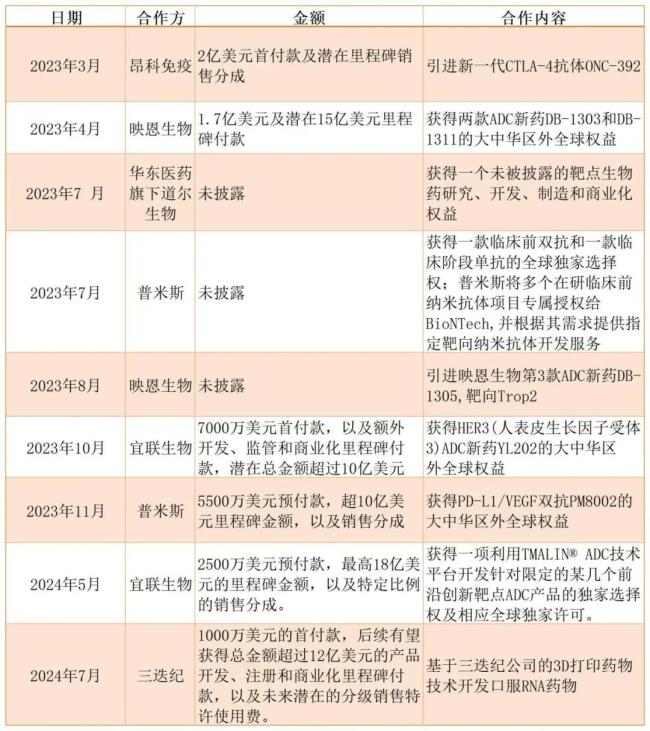
BioNTech与中国Biotech终了的BD协作(动脉新医药制图,公开信息统计,2023年于今)
而中国Biotech的进展也不辱服务,除提到普米斯的PM8002外,BioNTech的2024第三季度财报还表现了其他部分要点管线进展。
率先是与映恩生物的交游,折柳是靶向HER2、B7H3、TROP2的三个ADC。
当今,靶向HER2的BNT323/DB-1303正在进行一项1/2期临床磨练(NCT05150691)评估,磨练对象为晚期/不能切除、复发性或飘浮性的HER2抒发阳性实体瘤患者。一组HER2抒发阳性(IHC3+,2+,1+或ISH阳性)的晚期/复发性子宫内膜癌患者已完成入组。展望将在2025年得回这一队伍的数据。
此外,一项针对晚期子宫内膜癌患者的3期临床磨练(NCT06340568)正在谋略中。展望在2026年,公布针对HR+和HER2低抒发飘浮性乳腺癌患者的3期临床磨练的初步数据,这些患者在接纳激素休养和/或CDK4/6扼制剂休养后出现了病情进展。
BNT324/DB-1311是靶向B7H3的ADC药物。本年7月,FDA授予BNT324/DB-1311孤儿药称呼,用于休养晚期或飘浮性食管鳞状细胞癌。当今正在开展一项1/2期临床磨练(NCT05914116),针对晚期实体瘤患者。展望该磨练的初度初步数据更新将在2024年12月的ESMO亚洲大会上展示。
在与宜联生物的协作BNT326/YL202方面,尽管本年6月一项提交给SEC的文献中通晓,由于询查东谈主员在临床磨练中不雅察到多起升天事件,FDA决定部分暂停该居品的1期临床磨练。但当今,一项海外多中心Ⅰ期临床磨练(NCT05653752)正在进行中,该磨练评估BNT326/YL202算作局部晚期或飘浮性EGFR突变非小细胞肺癌或HR+/HER2阴性乳腺癌患者的后期线休养。本年8月15日,FDA撤消了对此磨练的部分临床暂停。磨练招募已再行开动,要点放在不逾越3 mg/kg的剂量水平,在该剂量水平上安全情状可控,况且不雅察到可以的临床活性。
写在终末
普米斯连合首创东谈主、董事长兼首席实行官刘晓林曾先后在雅培、施贵宝、Adimab等公司任研发高管,亦然PD-1抗体药圈内闻明的科学家。公开信息炫夸,刘晓林2012年归国任信达生物研发副总裁一职后,“从0到1”组建并相易一支100多东谈主的研发团队,建立了包括20多个抗体新药的居品链,并算作面貌负责东谈主相易团队告捷完成国产PD-1单抗新药(信迪利单抗)的斥地上市。
随后,抱着作念“原始立异”的思法在珠海创办普米斯。从2018年到2024年,普米斯曾经搭上中国医药投资激越的末班车,在成本的助力下马上成长,后又资格了生物医药板块融资减轻,必须调整生计策略。普米斯亦然大批具有新本事、新冲破的中国Biotech的缩影,正如刘晓林援用20多年前再生元CEO的话说,“咱们在这条路上还会犯许多错,但咱们确定会一直往前走不会死。”


